Die Chancen im Unbekannten

Die Chancen im Unbekannten
Jacob Corn entwickelt an vorderster Front Genom-Editierungstechnologien zur Heilung von Erbkrankheiten und forscht zum besseren Verständnis der menschlichen Gesundheit.
Woran arbeitet Ihre Gruppe an der ETH?
JACOB CORN – Einerseits entwickeln wir neue Technologien zur Genom-Editierung, mit dem Ziel, genetische Krankheiten zu heilen. Andererseits wollen wir besser verstehen, welche Auswirkungen diese Eingriffe im menschlichen Körper haben. Die meisten Editierungssysteme, um die es hier geht, verändern die Körperzellen des individuellen Patienten, indem sie gezielt Teile des Genoms modifizieren. Diese Prozesse erzeugen Schäden, die von den Zellen repariert werden müssen. Wir versuchen herauszufinden, wie Zellen DNA-Schäden reparieren, um präzisere und sicherere Editierungssysteme zu entwickeln. Ein weiterer Forschungsbereich beschäftigt sich mit der Frage, wie Zellen ihre eigenen Bestandteile abbauen und verwerten, insbesondere unter Stress oder im Alterungsprozess. Diese Mechanismen spielen eine Rolle bei vielen chronischen Krankheiten und bieten Potenzial für zukünftige Therapien.
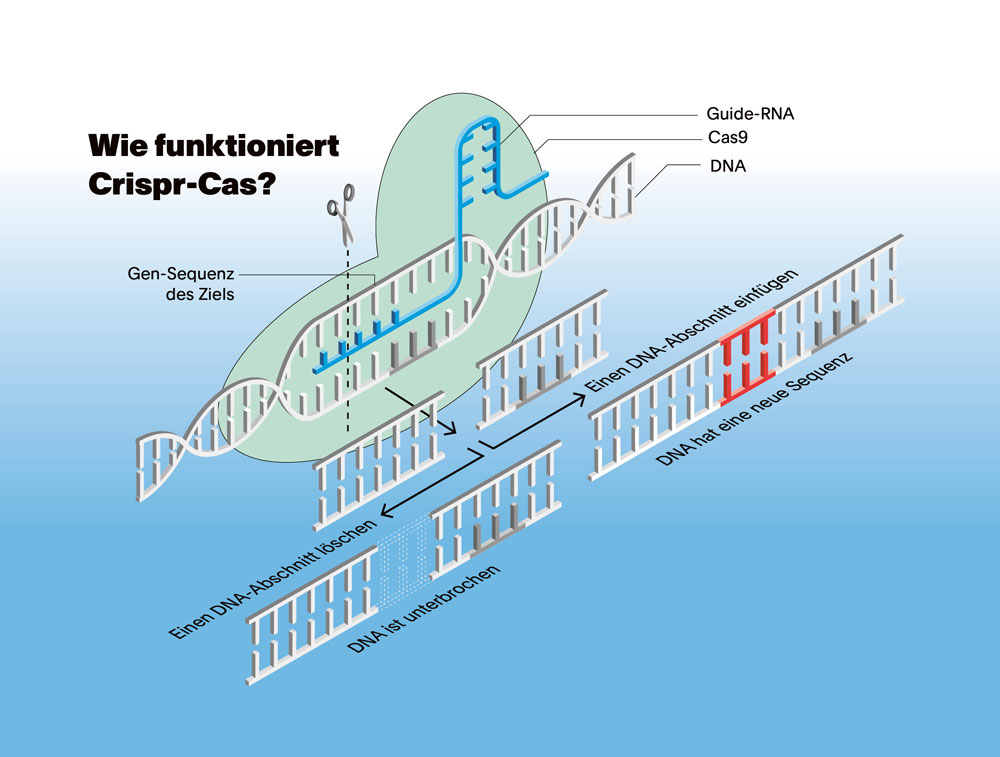
© Adobe Stock / ETH Foundation
Sie sind seit vielen Jahren einer der führenden Forscher in der Genombiologie. Wie hat die Entdeckung der Genschere Crispr-Cas Ihr Feld verändert?
Für mich ist die Entwicklung von Crispr-Cas ein Beispiel für die Demokratisierung von Wissenschaft. Genom-Editierung gibt es seit 1990. Die Editierungssysteme waren jedoch sehr langsam und ressourcenintensiv. Sie waren einer kleinen Gruppe von Spezialisten vorbehalten. Das Crispr-Cas-System hat die Technologie stark vereinfacht. Heute können Biologinnen, Mediziner oder sogar Studierende, die sich mit genetischen Krankheiten beschäftigen, diese Werkzeuge nutzen. So entsteht viel Raum für spannende Ansätze, unser Forschungsfeld hat sich stark beschleunigt. Der Fokus liegt nicht mehr nur auf der Technologie, sondern darauf, wie sie eingesetzt wird – sei es zur Heilung von Krankheiten oder zur Erforschung bis anhin unbekannter biologischer Mechanismen. Dies bringt natürlich auch neue ethische und sicherheitstechnische Fragen mit sich, die sorgfältig abgewogen werden müssen.
Sie und Ihre Gruppe forschen sowohl an pharmazeutischen Anwendungen als auch grundlagenorientiert. Welchen Stellenwert hat für Sie die Grundlagenforschung?
Sie ist entscheidend! Grundlagenforschung bildet die Basis von angewandter Forschung. Die Entdeckung von Crispr-Cas ist ein gutes Beispiel für die grosse Rolle, die Grundlagenforschung für unsere Gesellschaft spielt, denn sie entstand aus Erkenntnissen der mikrobiologischen Grundlagenforschung. Aufbauend darauf wurden innerhalb von wenigen Jahren vielfältige Anwendungsmöglichkeiten entwickelt.
Welche Krankheiten stehen im Fokus Ihrer angewandten Forschung?
Wir forschen an Heilmethoden für erbliche Blutkrankheiten, beispielweise der Sichelzellenanämie. Genetische Blutkrankheiten sind in Europa rar, weltweit sind jedoch fast 400 Millionen Menschen betroffen. Für mich persönlich steht ausserdem nicht in erster Linie die Prävalenz einer Krankheit im Vordergrund. Viele Krankheiten, die häufig vorkommen, wie eine bakterielle Infektion, können mit zahlreichen Medikamenten behandelt werden. Mutationen im Erbgut hingegen können heute durch DNA-Sequenzierung zwar erkannt werden, eine Heilung gibt es bisher jedoch nicht. Meine Vision ist, dass eines Tages Kinder mit seltenen Erbkrankheiten nicht nur diagnostiziert, sondern geheilt werden können.
Wie findet angewandte Forschung den Weg von Ihrem Labor in die Klinik?
Ein Weg ist, ein Spin-off zu gründen. Dies macht nicht nur die Weiterentwicklung vielversprechender Therapien möglich, sondern ist auch für die Wirtschaft relevant: Ein ehemaliger Doktorand, der ein Unternehmen startet, schafft Arbeitsplätze und generiert so Wertschöpfung. Es ist toll, dass solches Unternehmertum durch das Pioneer Fellowship an der ETH stark gefördert wird. Neben Jan Nelis mit Immitra Bio, der eine Plattform für Gentherapien entwickelt, kann aktuell Lilly van de Venn dank der Förderung ihre Methode für die Detektion von Off-Target-Effekten der Genom-Editierung – unbeabsichtigten Veränderungen im Genom – weiterentwickeln. Wir setzen zudem stark auf Kollaborationen mit der Klinik. Oft kommen Ärztinnen oder Ärzte mit konkreten Fragestellungen auf uns zu, und wir erforschen in der Folge neue therapeutische Ansätze.
Wieso ist die ETH Zürich der richtige Ort für Ihre Forschung?
An der ETH finde ich einen einzigartigen Mix aus Grundlagenforschung und technologischen Entwicklungen Tür an Tür. Dieses Umfeld ist sehr inspirierend. Zudem vereint die ETH herausragende Köpfe mit moderner Infrastruktur, ist sehr international und gut vernetzt. Die Nähe zu erstklassigen Kliniken wie dem USZ oder dem Kinderspital und zu hervorragenden anderen Bildungs- und Forschungsinstitutionen bildet den perfekten Nährboden.
Ihre Professur wird von der NOMIS Foundation sowie der Lotte und Adolf Hotz-Sprenger Stiftung gefördert. Was bedeutet diese Unterstützung für Sie?
Die Unterstützung, die wir von Stiftungen und von Gönnerinnen und Gönnern der ETH Foundation erhalten, ist von unschätzbarem Wert. Klassische Fördergelder sind meist an klare Vorgaben gebunden, und oft müssen die erwarteten Ergebnisse bereits im Förderantrag stehen. Doch bahnbrechende Entdeckungen entstehen dort, wo wir das Unbekannte mit offenem Ausgang erforschen. Freie Mittel aus philanthropischer Unterstützung ermöglichen genau die Art von visionärer Forschung, die uns die Chance gibt, wirklich neue Wege zu gehen.
Zur Person
Jacob Corns Erfahrungen verbinden Wissenschaft und Industrie und decken therapeutische Bereiche wie Infektionskrankheiten, Neurobiologie und Onkologie ab. Er promovierte 2008 an der University of California in Berkeley und startete seine Forschungskarriere als Gruppenleiter beim Biotechunternehmen Genentech. Danach kehrte er als wissenschaftlicher Gründungsdirektor des Innovative Genomics Institute und Dozent an die UC Berkeley zurück, bevor er 2018 an die ETH Zürich kam.


